江西牵头干扰素省际联盟集采来袭!
时间:2023-10-31人气:作者: 药闻康策
10月27日,干扰素省际联盟集中带量采购领导小组办公室发布《干扰素省际联盟集中带量采购文件(征求意见稿)》,除江苏、广东外,其余29省组成干扰素省际联盟,对15个干扰素药品进行带量采购,采购周期为4年。
01
采购品种
采购品种目录
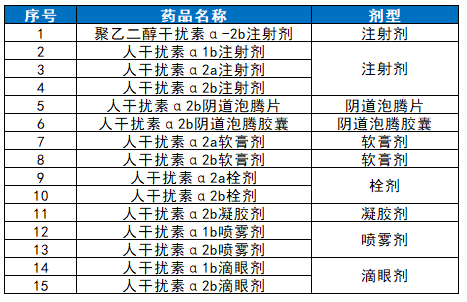
02
采购周期
3.采购周期内若提前完成当年约定采购量,超过部分中选企业仍按中选价格及时足量进行供应,直至采购周期届满。
03
集中采购当事人
1.申报企业
1.1 申报企业参加本次带量采购应当具备以下条件:
(1)具有履行协议必须具备的能力;
(2)参加本次药品集中采购活动前两年内,在药品生产活动中无严重违法记录;
(3)对药品的质量负责,一旦中选,作为供应保障的第一责任人,及时、足量按要求组织生产,并向配送企业发送药品,满足医疗机构临床用药需求;
(4)本采购文件规定的其他条件。
1.2 申报企业应按照采购文件的要求编制申报材料,申报材料应对采购文件提出的要求和条件做出实质性响应。
2.其他要求
2.1 若申报企业明显不具备申报资格中规定必须满足的全部要求,或涉嫌不如实提供证明材料的,一经确认,联盟集采办公室将不接受其申报;情节严重的,取消该企业生产的所有药品在采购周期内、联盟地区范围内药品集中采购活动的参与资格。
2.2 参加本次药品集中采购供应的药品,应是临床常用规格包装。
2.3 联盟集采办公室可根据工作需要对拟中选企业的药品拟中选药品质量进行调查(调查形式根据实际情况确定),拟中选企业应予以积极配合。
2.4 申报企业中选后,须按联盟地区要求签订购销协议。履约期间,中选企业原则上应确保持续拥有中选药品的国内有效注册批件,否则视为放弃中选资格。如确有需要变更药品上市许可持有人的,须提前向联盟集采办公室报告,按以下规则处理:
2.4.1 申报信息公开日前,已向药监部门申请变更药品上市许可持有人,可由当前药品上市许可持有人参与申报,申报产品资料须同时提供转让企业、受让企业双方盖章确认的承诺函,转让企业、受让企业信用评价等级等以严重程度更高者认定。转让、受让企业任意一家被列入“违规名单”的,该申报行为视同受“违规名单”条款约束。中选后获得药监部门批准变更,且最终批准结果与前期承诺内容一致的,则变更后的药品上市许可持有人可视为中选企业。
2.4.2 申报信息公开日后,中选企业向药监部门申请变更药品上市许可持有人并被批准的,视为放弃中选资格,并按第二部分第23条款给予相应处罚,备供企业按有关程序获得中选企业身份。
2.5 申报企业中选后,须按各地要求签订购销协议。履约期间,中选企业应确保持续拥有中选药品的国内有效注册批件,否则视为放弃中选资格。
2.6 中选药品在履行协议中如遇国家政策调整或不可抗力,致使直接影响协议履行的,协商解决。
2.7 申报同品种的不同企业,存在以下情形的,涉及企业的实际申报数计为1家,即视为1家企业参与投标和评审。涉及企业可自愿组成联合体作出承诺,授权其中一家企业为代表进行联合申报,评审以被授权的企业为准。如涉及企业独立或组成多个联合体进行申报,仅以差比后报价最低的企业视作有效申报,参与评审:
2.7.1 企业负责人为同一人或存在直接控股等情形;
2.7.2 包括但不限于工业和信息化部《2021年中国医药统计年报》化学制药分册中“化学药品工业企业法人单位隶属关系后注”确认的企业关系的情形(有相关文件证明企业间关系已改变的情况除外);
2.7.3 企业之间存在该品种有效注册批件转让的情形;
2.7.4 企业之间就该品种存在境外药品上市许可持有人境内代理人关系的情形。
04
申报报价
1.申报价的货币单位为人民币(元),保留小数点后2位;以最小包装(如:盒)为申报价单位。
2.申报价为申报企业实际供应医疗机构的价格,应充分考虑药品流通环节的相关费用,包括税费、配送费、退货、破损等在内的所有费用。同品种申报多个规格包装的,申报企业仅须选择任意一个规格包装进行申报报价。
3.申报价按药品差比价规则折算至最小制剂单位(片/粒/支/瓶/袋)后作为“最小制剂单位报价”(四舍五入保留小数点后4位)。
4.申报企业确认并提供“符合申报条件的供应品种清单”,相关中选药品价格由联盟集采办公室以本企业拟中选产品的申报价参照药品差比价规则计算确定。
5.本次集中采购所涉药品差比价关系参照现有规则,根据剂型、规格(装量差异按照含量差比价计算)、包装数量计算,不考虑包装材料差异,不考虑冻干粉针、溶媒结晶粉针与小容量注射剂的差异。同品种中,同规格预灌封包装与安瓿瓶(西林瓶)包装的差额以2.5元计,同规格带安全装置预灌封与安瓿瓶(西林瓶)包装的差额以3元计。
05
拟中选企业确定
注:降幅计算公式为:降幅=(同品种最高有效申报价-报价)/同品种最高有效申报价*100%。降幅保留2位小数(四舍五入法)。
06
供应地区确认
1. 同品种有效申报企业在3家及以上的拟中选企业进行主供地区和备供地区确认。若拟中选企业未按时参与供应地区确认,视同放弃拟中选资格。
2. 主供地区确认。拟中选企业首先进行主供地区确认程序,第一顺位企业优先在供应地区中选择1个地区。优先选择完毕后,从第一顺位企业开始,所有拟中选企业按顺位依次确认剩余地区,每个拟中选企业每次选择1个地区,重复上述过程,直至所有地区选择确认完毕。
3.备供地区确认。拟中选企业在主供地区确认完毕后,按中选产品顺位进行备供地区确认程序。每个拟中选企业的备供地区须不同于其主供地区。
07
2.3 中选企业只有1家时,获得同品种80%需求量。
08
流标品种未中选药品处理
流标品种和未中选药品将在省级医药采购平台予以单独标识,其采购情况纳入重点监测范围并定期通报。公立医疗机构采购流标品种或未中选药品时应予以报告说明。
09
中选企业中选价格的动态调整
1.中选价格调整
在本次集采周期集采中选结果执行一个完整采购年度后,根据实际使用量与上一采购年度实际使用量的比值(Q值),且当该企业中选产品的归属净利润增长率≥0,启动中选价格的调整机制。(1)Q值≤110%,中选价不作调整。(2)110%<Q值≤140%,中选价下调5%。(3)140%<Q值≤170%,中选价下调10%。(4)170%<Q值≤200%,中选价下调15%。(5)Q值>200%,中选价下调20%。
2.中选品种归属净利润增长率
在执行周期,中选企业在每个采购年度结束后,根据联盟集采办公室通知要求,及时填报中选品种经过第三方审计的归属净利润增长率,报送至联盟集采办公室。
3.定期通报采购进度
联盟地区应按年通报中选产品使用情况进度,并将通报结果通报报送联盟集采办公室。
END
(来源:华招医药网)
标签:
【免责声明】
1.“高鹏说药材”致力于提供中药行业各类资讯信息,但不保证信息的合理性、准确性和完整性,且不对因信息的不合理、不准确或遗漏导致的任何损失或损害承担责任。
2.“高鹏说药材”部分文章信息来源于网络转载是出于传递更多信息之目的,并不意味着赞同其观点或证实其内容的真实性。如对内容有疑议,请及时与我平台联系。
3.“高鹏说药材”所有信息仅供参考,不做任何商业交易及或医疗服务的根据,如自行使用“高鹏说药材”内容发生偏差,我平台不承担任何责任,包括但不限于法律责任,赔偿责任。
4.“高鹏说药材”各类带“原创”标识的资讯,享有著作权及相关知识产权,未经本网站协议授权,任何媒体、网站、个人不得转载、链接或其他方式进行发布;经本网协议授权的转载或引用,必须注明“来源:高鹏说药材(www.gpsyc.com)”。违者本网站将依法追究法律责任。
5.本声明未涉及的问题参见国家有关法律法规,当本声明与国家法律法规冲突时,以国家法律法规为准。
最新文章

药材行业烂摊子怎么破?这位老党员砸了铁饭碗,搞了三个“猛项目
朋友们,做药材的、搞健康产业的,最近是不是感觉特别难?药材价...(915 )人阅读时间:2025-09-25
坦白讲!中医养生这么火,但不懂行千万别瞎搞!
朋友,你是不是也瞅着中医养生这波热潮,心里痒痒的?但一想到水...(563 )人阅读时间:2025-09-25
高久恒说药材寻创业合伙人:一起把老祖宗的好东西,变成这个时代
一、平台简介:高久恒说药材——您身边的中医药创业引路人在健康...(768 )人阅读时间:2025-09-25
高久恒说药材寻创业合伙人:一起把老祖宗的好东西,变成这个时代
一、平台简介:高久恒说药材——您身边的中医药创业引路人在健康...(704 )人阅读时间:2025-09-24


 红星资本局6月27日消息,中药材价格涨势迅猛引发多方关注。相...
红星资本局6月27日消息,中药材价格涨势迅猛引发多方关注。相... 企业名称铁岭鹿宝堂药业集团有限公司企业类型药品生产企业检查时...
企业名称铁岭鹿宝堂药业集团有限公司企业类型药品生产企业检查时...
 4月24日,在第五届医药创新生态大会的中药创新发展论坛上,中...
4月24日,在第五届医药创新生态大会的中药创新发展论坛上,中...




