中药材及饮片质量标准研究有关问题思考
时间:2022-07-12人气:作者: 中药材种植养殖专业委员会

中药材及饮片质量标准研究有关问题思考
魏锋,程显隆,荆文光,陈佳,余坤子,张萍,严华,李明华,杨建波,马双成*
(中国食品药品检定研究院,北京102629)
摘要:中药材及饮片是中医药事业传承和发展的物质基础,其质量优劣直接关系到中医临床用药的有效性和安全性。中药材及饮片质量标准是中药质量控制和评价的依据,同时对中药质量提升具有推动和引领作用。但由于中医药理论极其深奥,中药防治疾病的机理研究和认识还不够深入系统,对中药的质量认识还不够全面,导致标准研究制修订工作中科学依据不足,因而标准的科学性、合理性和实用性往往受到争议和质疑。本研究通过梳理近年来中药材及饮片的质量概况,对标准研究中存在的一些突出问题进行分析,提出了符合中药材及饮片质量特点的标准制定原则:一是坚持中医药特点,基于中医临床质量认知,制定有效的标准;二是坚持中药材质量特点,围绕质量属性确立质量指标,制定管用的标准;三是守住真伪和安全底线,基于风险评估,制定安全的标准。本研究对中药材及饮片质量标准研究常见问题和认识误区进行了分析讨论,强调了标准不仅是供检验和监管用,更是为了指导中药材和饮片生产、流通、使用全过程的技术遵循,应注重标准的科学性、合理性、可行性。同时,标准对中药材资源可持续利用及中药产业高质量发展具有引导和推动作用。最后,从质量提升和完善标准的角度,建议加强全产业链生产技术规范和标准完善,同时加强质量评价标准研究,以道地性和生产规范性生产基地建设为引擎,使新颁布的《中药材生产质量管理规范》落地见效,从源头和根本上提升中药材质量,保障中医药事业高质量发展。
关键词:中药材及饮片;质量标准研究;研究原则;有关问题
Some concerns about the standard establishment of Chinese medicinal medicines and decoction pieces
WEI Feng, CHENG Xian-long, JING Wen-guang, CHEN Jia, YU Kun-zi, ZHANG Ping, YAN Hua, LI Ming-hua, YANG Jian-bo, MA Shuang-cheng*
(National Institutes for Food and Drug Control, Beijing 100050, China)
Abstract: Chinese medicinal materials and decoction pieces are the material basis for the inheritance and development of traditional Chinese medicine (TCM). Their quality is directly related to the effectiveness and safety of TCM clinical practice. Quality standards can promote and guide the quality control, evaluation, and quality improvement of TCM. However, due to the profound theory of TCM, the mechanism of TCM prevention and treatment of diseases is not in-depth and systematic, lead to lack of scientific basis for the standard research and revising work, scientific nature, rationality and practicability of the standard is often questioned. This paper analyzed the outstanding problems existing in the standard study, such as weak correlation between standard indicators and quality attributes,and unreasonable acceptable limit, and put forward the standard formulation principles in accordance with the quality characteristics of Chinese medicinal materials and decoction pieces: First, adhere to the characteristics of TCM theory, based on TCM clinical quality recognition, formulate effective standards; The second is to adhere to the quality characteristics of Chinese medicinal materials, establish quality indicators around quality attributes, and establish effective standards; Third, we should guard the bottom line of authenticity and safety, and formulate safety standards based on risk assessment. This paper analyzed and discussed the common problems and misunderstanding in the study of quality standards of Chinese medicinal materials and decoction pieces and emphasized that the standards are not only for inspection and supervision, but also for guiding the technical compliance of the whole process of production, circulation and clinical use of Chinese medicinal materials and decoction pieces, and should be scientific, reasonable and feasible. At the same time, the standards can guide and promote the sustainable utilization of TCM resources and the high-quality development of TCM industry. Finally, from the perspective of quality improvement and perfect the standard, Suggestions to strengthen the whole industry chain production technology norms and standards, strengthen the quality evaluation standard research, at the same time with the construction of Daodi authentic and standardized production bases as the engine, the newly promulgated " Good Agriculture Performance of Chinese medicinal materials production " will be implemented and effective, so as to fundamentally improve the quality of Chinese medicinal materials and ensure the high-quality development of traditional Chinese medicine.
KEY WORDS: Chinese medicinal materials and decoction pieces; standard establishment; the standard formulation principles; concerns and suggestions
1.中药材及饮片的质量概况
中药材是中药工业的生产原料,是中医药事业传承和发展的物质基础,是我国独特且具有战略意义的宝贵资源。中药饮片是以中药材为原料生产的中医临床处方用药,同时也是中药制剂的原料。因此,中药材及饮片的质量是中医临床用药安全有效的基础和保障。质量源于生产,源头控制及全链条生产过程的规范是质量的保证,加强中药材及饮片的标准制定、规范生产、全过程控制和市场质量监管,对促进中药全产业链质量提升具有根本性、基础性作用。近年来,随着中药材及饮片基础研究逐步深入,生产技术不断进步,标准体系逐步完善,市场监管持续加强,以及全行业质量意识的不断提高,中药材及饮片的质量水平也逐年提升。从全国市场质量抽检数据看,2013~2021年我国中药材及饮片总体合格率分别为:64%、68%、75%、77%、84%、88%、91%、96%、97%,呈现出逐年提升、稳步向好的发展态势[1],应该说当前中药材及饮片生产供应和质量情况基本满足了中医药临床用药、中药产业和健康服务业快速发展的需要。同时,也要看到中药材产业发展仍面临着严峻挑战:一方面由于土地资源减少、生态环境恶化、过度采挖和利用,导致部分野生中药材资源流失、枯竭;另一方面中药材生产技术相对落后,生产规范性不够,公众对高品质中药的需求与中药材质量难以提升、优质中药供给不足之间的矛盾日趋凸显。人工种植环节出现的不适宜产区栽培、种植年限不够、采收加工随意、滥用化肥农药及生长调节剂等暴露出重产量轻质量,以及追求药典标准“及格率”的现象较为普遍。因此,质量抽检数据显示的市场监管合格率提升,并不能掩盖高合格率下中药整体质量重心下移的事实,特别是中药材品质重心下移的难题(图1),仍是制约中药质量和临床疗效发挥的最大掣肘,在一定程度上不仅损害了中医药信誉,更与我国中药产业高质量发展的目标背道而驰。
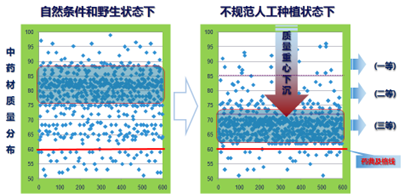
2.中药材及饮片标准有关问题
药品标准是对药品质量规格及检验方法所做出的技术规定,是药品研究、生产、经营、使用、检验及监管共同遵循的法定依据。标准是实施标准化的前提和基础,对推动和引领中药质量提升具有决定性的作用,而标准化是中药规范化、规模化、现代化以及可持续发展的保证。“标准决定质量,有什么样的标准就有什么样的质量,只有高标准才有高质量”,“质量提升,标准先行”,促进和发挥中药材及饮片标准的引领作用,切实提升中药材和饮片质量水平,是推动中药产业规范化、规模化和现代化发展的前提。《“十四五”中医药发展规划》更强调提升中药质量控制水平对于满足临床用药需求,满足人民群众日渐增长的多样化健康需求,促进中药产业高质量发展具有重要意义。按照标准化管理要求,药品须按规范(GMP、GAP)生产,药品标准通常是针对规范生产条件下的产品质量规格,而对于野生为主的中药材,鉴于其自然属性,事实上很难制定标准或进行标准化管理。因此,中药材标准除了发挥质量控制作用外,还有鼓励和推动规模化、规范化人工种植的导向。目前大多数常用中药材品种以人工种植/养殖为主,一些少常用品种以野生为主,加之中医药理论深奥、中药基础研究薄弱、质量影响因素多、评价难度大等原因,中药材标准制定和质量控制方面仍然存在不少问题,标准“不好用,不管用”的问题仍然突出,亟需完善和提高,全产业链标准化工作任重道远。
2.1标准对提高中药质量和保障公众用药安全发挥了重要作用
我国中药材及饮片标准由国家标准和地方标准两级标准组成,近年来随着中药基础研究工作的逐步深入以及中药质量控制技术水平逐步提高,中药材及饮片的标准也越来越完善,标准在指导和促进规范生产、提高质量、保障安全、服务监管等方面均发挥了重要的作用。以《中国药典》中药材及饮片标准为例,2020年版重点完善了中药饮片标准体系,对于饮片炮制项为净制、切制的,经过对性状、鉴别、检查等项目的系统研究,大多数品种加以修订完善。同时对于经炮炙或其他处理后的饮片,在科学研究的基础上,进一步加强专属性的质量控制项目,突出了中药炮制“生熟异治”的特色;在安全性控制和保障人民用药安全方面,根据当前中药材和饮片生产中存在的农药不规范使用、重金属超标、发霉变质导致真菌毒素超标等问题,全面提升了安全性控制水平,如完善了“中药有害残留物限量制定指导原则”,新增“药材及饮片(植物类)中33种禁用农药多残留测定法”,制定了33种禁用农药的控制要求,制定了中药材及饮片(植物类)重金属及有害元素的限量标准,作为指导性要求[2]。对容易发霉变质的蜂房、土鳖虫等中药材品种,增加了黄曲霉毒素的限量要求,薏苡仁增加了玉米赤霉烯酮的限量要求。针对马兜铃酸类成分具有潜在肾毒性的问题,2020年版《中国药典》不再收载含马兜铃酸类成分含量较高的马兜铃和天仙藤两个药材。此外,在国家政策的推动下,各地纷纷开始完善地方中药材和中药饮片质量控制体系,陆续修订和完善了地方药材标准和中药饮片炮制规范。整体来看,我国中药材及饮片标准在科学性、规范性、完整性等方面进步明显,中药质量和安全控制水平均有显著的提高。
2.2标准研究中存在的一些突出问题
由于基础研究薄弱加上中药材及饮片天然影响因素多、质量控制难度大等多方面特殊原因所致,我国中药材及饮片的标准仍然存在许多不足。特别是在分析方法的科学性、指标选择及限度制定的合理性、标准的实用性和可行性等方面仍然需要不断研究,持续提高和完善,突出问题主要表现在以下几个方面。
2.2.1指标和质量相关性不强
中药材及饮片质量指标是与质量影响因素密切相关,可用于定性或定量表达其质量属性(如有效性、安全性、稳定性、一致性、真实性等)的系列代表性质量参数或特性。为了确保中药材及饮片应有的质量属性,质量指标应尽可能反映其来源或身份的正确性和真实性、生产过程的规范性、以及产品真伪优劣等方面的综合质量特性。因此,质量标准研究工作中质量指标的确立非常关键,质量指标的选择时要考虑与中药材或饮片质量属性相关性强、代表性好、实用性强的指标。但多数标准研究制定过程中,对中药材质量属性形成规律不清楚、影响质量的核心因素不了解、质量控制关键点把握不准,进而造成质量指标的确立和选择存在片面性、主观性、随意性,因而其科学性和合理性屡受质疑。如有一些含量测定指标成分的确立仅仅是因为其在某一方面具有细胞活性而被确立为药材或饮片的“有效成分”,有一些指标是因为容易获得含量测定的对照品或因为其在药材中的含量最高而被确立为质量指标。所选定指标与中药材及饮片质量属性形成因素,如产地、生长年限、采收加工和炮制生产的规范性等重要因素的关联性存疑,导致制定的标准无法控制和评价质量,自然也无法指导行业内规范生产,市场监管时面对检验不合格的产品也说不上原因,缺乏底气,行业内也不知道如何改进提高,以确保下次“合格”。比如酸枣仁的标准,含量测定项要求测定酸枣仁皂苷A(不得低于0.030%)和斯皮诺素(不得低于0.080%)。日常检验曾遇到一批酸枣仁检品,其酸枣仁皂苷A符合限度要求,而斯皮诺素为0.076%,达不到标准限度规定,只好判定该批酸枣仁不合格。从外观性状看,该批酸枣仁为干燥成熟种子,无掺伪,性状和鉴别等其他检验项目均符合规定。酸枣仁皂苷A和斯皮诺素均为酸枣仁的微量成分,和酸枣仁中其他众多已知或未知成分一样,或多或少会有某一方面的生物活性,但斯皮诺素的含量高低和酸枣仁的质量形成因素(成熟程度、采收时间及加工规范性、发霉变质等包装贮藏规范性等)的相关性究竟如何评价?不是很清楚。当含量测定指标造成产品不合格但又无法解释其质量原因时,这样的质量指标宁可不列入标准,因为质量指标无法指导行业生产出“斯皮诺素合格”的酸枣仁,更无法生产出高质量的酸枣仁,反而会让行业无所适从,市场监管自然也无底气,难硬气。因此,从质量控制和评价的角度,在制定标准时应该选择与药材内在质量相关性强、代表性好的指标为宜。
2.2.2质控指标限度制定欠合理
限度的合理性决定于我们对质量水平的可接受程度及制定限度所测样品的代表性。一些涉及安全性方面的限度,需要基于风险评估。一些涉及纯净度、成分含量或稳定性等方面的指标和限度需要结合产品的质量特点、对质量水平的基本要求、产业发展水平和成本效益综合分析等。在中药材及饮片标准研究和制定工作中,取样的代表性不足往往是导致限度制定欠合理的主要原因。例如行业内反映较多的《中国药典》炒紫苏子饮片水分限度合理性问题,标准规定为不得过2.0%,日常检验的确发现炒紫苏子的水分经常会达到3%~4%,导致市场产品难以合格。这可能与标准制定过程中选用的样品代表性不足有关系,比如南方北方地域代表性、产品新旧或放置时间的代表性、产品炒制方法或工艺的代表性、产品包装贮藏条件的代表性等等都应该予以考虑。
此外,限度的合理性往往是质量要求和行业生产规范程度之间的博弈和平衡。在有些情况下,标准不能跟着市场走,特别是当产业界存在一些影响质量的不规范行为时,标准应坚守质量底线。例如,近年来市场上五加皮饮片灰分检查项和浸出物测定项不合格率较高,因此标准中灰分检查和浸出物限度制定的合理性受到行业内的质疑。我们研究发现其灰分和浸出物项不合格主要有3方面原因:①与采收加工清洗不干净有关。按照《中国药典》中“五加皮”项下要求,夏、秋二季采挖细柱五加根部,洗净,剥取根皮,晒干。如果细柱五加根部清洗不干净,可能会导致总灰分和浸出物不合格;②与种植年限有关。2年生的五加皮样品总灰分合格,但浸出物多不合格。而种植/野生4年或以上的五加皮浸出物和总灰分均合格;③与五加皮加工时抽芯不完全有关。细柱五加的根芯浸出物较低,总灰分也较低。如果抽芯不完全,总灰分容易合格,而浸出物会偏低。综上所述,建议细柱五加规范种植4年以上(事实上,两年或以下的五加皮多达不到药典性状项下“直径0.4~1.4cm,厚约0.2cm”的要求),采收加工时趁鲜清洗干净,抽芯完全,可基本确保五加皮的总灰分和浸出物符合2020年版《中国药典》质量要求[3],无需修订《中国药典》五加皮标准浸出物和灰分检查项的限度。因此,标准要起到规范和引领市场生产行为的作用,不能简单因为市场产品不合格率高就要求药典标准降低限度。
2.2.3饮片特色体现不足
饮片是中医临床的处方药,饮片的特殊炮制工艺和使用方式是中医特色的集中体现。目前饮片标准多基于药材标准质控指标的延用或个别指标限度的调整,多为中药材含量限度的降低。在指标的选择和限度制定方面没有充分体现饮片的特点和炮制工艺对质量的影响,因而饮片的质量特性体现不足,质量可控性不强,更难以评价其质量优劣。比如女贞子饮片有女贞子和酒女贞子(酒蒸法或酒炖法)两种规格,其临床功效特点和使用有别,女贞子生用强于清虚热,酒制后增强滋补肝肾的功效,同时可缓解生品女贞子所致滑肠泻下作用。然而在二者的质量控制标准方面,2015 年版《中国药典》没有加以区分,女贞子、酒女贞子均以特女贞苷作为含量测定的指标成分,且含量限度一致,均规定含特女贞苷不得少于0.70%,难以体现女贞子酒制的炮制原理,亦难以全面控制和评价酒女贞子的质量。实验证明,酒制过程对女贞子中所含的环烯醚萜类与苯乙醇类等化合物含量影响显著。随着蒸制时间延长其环烯醚萜类成分如特女贞苷的含量逐渐降低,而苯乙醇类化合物如红景天苷的含量呈现上升的趋势(图2)。显然,酒女贞子的质量控制指标应以红景天苷为宜,该指标既可以体现酒制品和生品的区别,其含量高低又可以反映酒制程度,炮制是否到位。如果饮片仍以特女贞苷为测定指标,会导致规范生产炮制到位的酒女贞子含量测定反而不合格[4-5],最终导致行业内不敢规范炮制,影响炮制品整体质量下降。鉴于此,2020年版《中国药典》已对酒女贞子的标准进行了修订,选用红景天苷为含量测定指标,使之更加科学合理,亦更能体现饮片炮制特色。
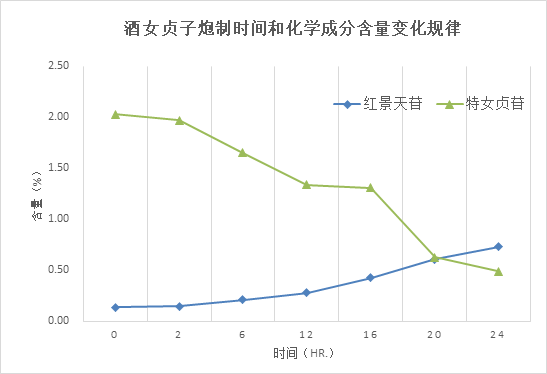
以上举例反映的仅是中药材及饮片标准研究制定过程中普遍存在的共性问题。从质量控制和质量管理的角度看,中药材及饮片的质量源于生产,不能把所有质量问题都归咎于药材或饮片标准的不完善,生产过程的规范性是质量的保证。由于中药材具有农产品的属性,其种植生产、采收加工、流通贮藏、以及饮片炮制等过程产业链条长,涉及的人员和部门多,质量受自然和人为的影响因素多,给质量控制和市场监管带来了很多困难。依据标准检验和执法是药品监管的常用手段之一,特别是近年来监管力度加强后,中药材及饮片标准受到了全行业空前的关注。当出现检验不合格的情况,作为检验依据的药品标准往往首当其冲受到科学性、合理性方面的质疑,行业内“标准不管用、不好用,设定的项目和指标与中药质量无关”等争议与质疑之声时有出现。可以说,在当前中药研究依然薄弱,有效物质基础不清和作用机理不明的条件下,中药质量标准承载了远远超出其标准本身功能范围的负荷。如何根据中药材及饮片的特点,厘清中药质量内涵,制定科学、合理、可行的标准,更好服务于生产、流通、使用和市场监管,更好服务于中医临床,成为中药质量控制和评价的重要任务和全行业亟待破解的难题,也是推动中医药创造性转化和创新性发展,加快推进中医药事业和产业高质量发展的关键。
3中药材及饮片质量标准研究基本原则和思路
3.1中药材及饮片标准研究主要内容和要点
标准研究和制定工作必须规范和严谨,以确保标准的科学性、合理性、可行性。中药材及饮片标准内容通常包括名称、来源、性状、鉴别(经验鉴别、显微鉴别、理化鉴别)、检查(水分、灰分、杂质、重金属及有害元素、农药残留、真菌毒素、有毒成分限量等)、浸出物、含量测定、炮制、性味与归经、功能与主治、用法与用量、注意、贮藏等。名称即是中药材名称或饮片名称,是药品最为重要的身份信息,也是中药生产、流通、临床使用、市场监管等共同遵循的标准信息。中药材名称包括中文名、汉语拼音及拉丁名。中药饮片加工方法仅为净制、切制的饮片名称通常同药材,采用炮炙加工方法的,名称中取炙法与药材名称相呼应。中药材或饮片名称的确定或修改须规范。另外,命名时须防止把中药材名称和药用植物名称混淆,比如中药“藿香”为常用知名中药,历代本草均为藿香名。其来源为唇形科植物广藿香Pogostemon cablin(Blanco)Benth.的干燥地上部分,据此将藿香的药品名称改为“广藿香”不妥,相当于沿用几千年并且至今很常用的中药藿香,在国家标准里没有名称和身份了。而且,中药材名称的修改涉及到饮片名称和成方制剂处方药味名称的改变,以及与本草文献记载的关联性和追溯性,因此,中药材饮片标准涉及命名及修订问题一定要慎之又慎。来源项包括基原、药用部位、采收季节、产地加工等信息,必要时收载产地、生长年限、传统名称和规格等。因为分类学在不断发展变化,中药材标准在基原方面须保持相对的稳定,对于非公认的、较新的、存在学术争议的、过细的分类研究结果不宜急于跟进盲目采用,因此药典来源项下关于基原的内容通常也会相对滞后一些。性状项主要描述药材的形状、大小、表面 (色泽、特征)、质地、断面、气味等特征。性状应根据样品的实际情况进行准确描述,性状描述的特征性内容,特别是大小、长短、厚薄、粗细等数值是通常情况下对大多数样品可药用部分共有特征的范围区间,并不是取最大和最小的极值区间,也不是量取药材某一个特定部位的数值。可允许少量样品超出范围,在制定标准和使用标准进行检验判定时均需注意。药材经过栽培或迁移后应当进行质量对比研究,对于栽培技术方法较为成熟、性状变异特征趋于稳定的变异情况,在药材质量符合药用要求的前提下,可以考虑适当将栽培品的性状描述纳入标准。鉴别是指对药材、饮片的真伪进行判定,包括经验鉴别、显微鉴别、理化鉴别(包括物理、化学、色谱、光谱、分子生物学方法等)。鉴别方法应强调专属性和重现性,尽可能区别同类相关品种或可能存在的易混淆品种。近年来较常用于标准的特征图谱/指纹图谱本身是一种技术方法,本质上属于鉴别项下的内容,不宜与标准中性状、鉴别、检查、含量测定等项目相并列。检查项主要包括安全性、均一性、纯度及稳定性等方面。应根据中药材及饮片各品种的特点设定具有针对性的检查项目,如伪品、混淆品、色素、色度、吸水性、发芽率等限量检查。制定检查限度时应收集具有足够代表性的样品,根据实测数据制定限度。安全性检查项限度制定需基于风险评估。浸出物系指根据药材、饮片中主要成分的理化性质采用水、乙醇或其他适宜溶剂进行提取测定。含量测定成分的选择应以临床功效为导向,选择与功能主治及活性相关的专属性成分作为含量测定指标,功效不明确或难以用个别化学成分表达时,建议选用和质量相关的指标性成分进行含量控制。饮片标准内容除了与药材相似的项目外,还增加了炮制、性味与归经、功能与主治、用法与用量、注意、贮藏等。理论上,饮片应该由合格的中药材炮制而成,因此饮片标准除体现其原料药材的质量属性外,还应当体现炮制工艺赋予饮片的质量属性。
3.2体现中药材及饮片质量特点的标准制定原则
在中药材及饮片标准研究中,应该结合药材、饮片的特点和质量属性相关规律,特别是在质量控制指标的确立和限度制定方面,应该突出强调或遵循的一些基本原则。结合近年来在标准研究制修订中常见的问题,为了提高标准的科学性、合理性和可行性,在中药材及饮片标准研究制定中首先应该坚持和遵循以下几方面的原则。
3.2.1坚持中医药特点,基于中医临床认知,制定有效的标准
坚持中医药特点并基于中医长期临床经验总结形成的中药质量观,是研究和制定中药标准的基本原则和前提,也是中药标准和现代植物药或天然药物标准制定思路的根本区别。我们通常所说的“道地药材”就是中医临床长期实践的总结和对中药质量最直接最有效的认知。中药材及饮片的传统性状特征(形状、大小、颜色、气味、质地等)往往隐含着产地信息、种植生长方式、生长年限、采收季节、加工方式、炮制工艺等质量要求。也是经过长期临床实践验证和经验总结出的质量认识。近年来在中药材的种植过程中,行业内出现了一些不遵循传统中药道地产区共识,盲目追求产量而轻视质量的跨区引种现象,“北药南移”“降低海拔”,或者有“年限不够”“抢青采收”等不规范情况。如防风药材种植区有从北方向南方引种的趋势,由于产地变化和种植方式的改变,药材的性状和内在化学成分均发生了较大的变化,野生防风的“蚯蚓头”、体轻、断面裂隙等特征在栽培品上看不到了,而栽培防风多分叉,质重、断面色浅无裂隙,二者在性状和主要化学成分及含量水平方面差别很大(图3)[6]。连翘因采收季节和成熟度不同,分为“青翘”和“老翘”,临床用途也各不相同。二者在浸出物、连翘酯苷A含量差别很大,因此标准分别对其制定了限度。但连翘随采收期延后其所含的一些化学成分如连翘苷、连翘酯苷等含量下降明显,因而存在青翘“抢青”现象[7]。为了控制行业内不规范的采收,经研究发现挥发油量随采收期推后而升高,八月中旬后达到稳定(大于2.5%),因此新版中国药典标准修订时增加了挥发油含量为指标成分,该指标与采收规范程度呈正相关,可有效控制青翘“抢青”采收问题[8]。
基于中医临床实践的总结和认知,确保道地性和生产规范性即是有效性的保证。因此,寻找道地产区和非道地产区(或适宜产区和非适宜产区)药材的质量差异,比较规范种植和非规范种植情况,如不同种植方式、生长年限、采收季节、加工方法、炮制工艺对中药材及饮片造成的质量差异,进而寻找与质量正相关的指标是制定有效标准的关键[9-11]。坚持中医药特点,还需强调中药有效性和安全性是整体效用的综合表现,不宜夸大个别化学成分或主要化学成分单方面的药理活性,质量标准应尽力体现中药材的整体质量概貌,从多质量属性的维度利用多指标、多技术手段进行综合全面控制,防止单一指标或唯成分论的片面性。

3.2.2坚持中药材质量特点,围绕质量属性确立质量指标,制定管用的标准
中药材不同于化学药,质量属性和特点鲜明,质量控制和评价难度大。首先,从质量属性形成的角度看,中药材自然属性强,其质量受环境因素影响大,其源头属农产品,生产环节链条长,因而质量影响因素多。其次,从中药功效特点看,因其所含化学成分多,作用方式多样,起效途径各异,作用机理复杂,再加上中药材及饮片均一性差,造成其质量控制和评价难度极大。另外,中药因其所具有的独特中医药理论体系、生物学属性、多样的存在形式、特殊的炮制加工、生产工艺和剂型特点、药效作用特点、使用特色及历史文化传统,其质量构成具有鲜明的自身特点,兼具自然属性和人文属性,因而其质量控制和评价又增加了特殊性和复杂性。
中药材及饮片因种植生产加工方式不同其客观上存在质量等级,但当前的标准却难以体现其质量差别,难以评价其优劣。近年来围绕中药质量控制和评价虽然研究思路多,但可行方法少,形成的标准争议也较多,中药材及饮片标准“指标和内在质量无关,无法控制质量,无法指导生产”等质疑声不断。“知道如何种出质量好的三七,也可以按三七药材进行质量分等,但药材打粉后三七粉没法区分质量等级”的尴尬局面仍然存在。质量“说不清”的困境在一定程度上也影响了中药市场秩序,造成质量优劣难辨,劣币驱逐良币,市场质量监管乏力、使不上劲、甚至底气不足。究其原因是本质上未找到真正的内在质量指标。这一问题已成为中药质量控制和评价的痛点,也是当前中药质量研究的学术瓶颈问题。
质量源于生产,生产过程的规范性是质量的保证。目前中药材及饮片的质量问题多由不规范生产引起。对于大多数常用中药材,我们基于临床经验积累和种植生产规律总结,其实已经大体把握质量优劣的形成过程和影响因素,也已经明确规范种植的质量优于不规范种植的,只是不清楚用哪些质量指标去识别和评价这些质量差异。因此,基于质量属性形成的关键环节和影响因素开展标准研究,寻找、发现、确立真正的质量指标,让质量指标和生产过程的规范性关联起来,所建立的标准方能是管用的标准,能够指导规范生产的标准和市场监管有底气的标准[12-13]。

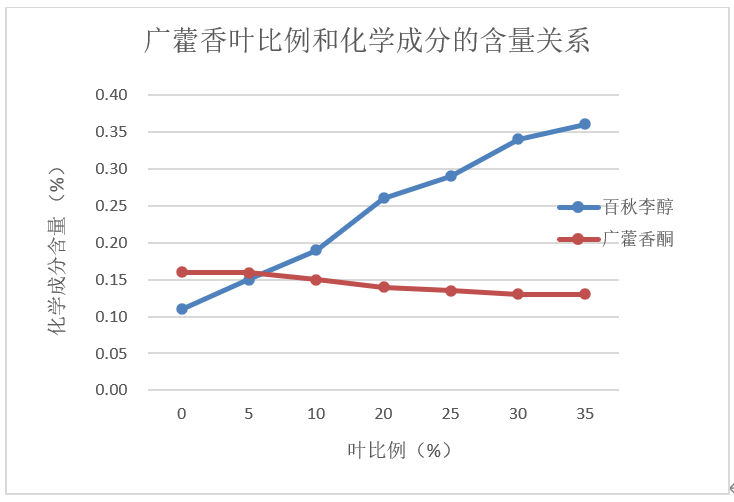
以广藿香药材及饮片标准研究为例。广藿香为芳香化浊,和中止呕,发表解暑常用药,中医临床认为其质量以“叶多,香气浓郁者佳”。然而2020年国家中药饮片抽检发现,大多数广藿香饮片只有梗,几乎看不到叶(图4),但按标准要求检验其百秋李醇含量,这些饮片均能达到药典制定的限度0.10%。按照药材采收加工和饮片炮制生产工艺,规范生产的广藿香饮片叶比例应为30%~40%。产地调研发现广藿香的叶多用于提取挥发油而很少投入饮片生产,这是饮片基本无叶的根源,而大多数饮片又能符合《中国药典》的质量指标,说明现行药典标准无法有效控制广藿香饮片的质量。对不同叶比例的广藿香饮片中百秋李醇含量测定发现,百秋李醇含量和饮片中叶的比例呈正相关(图5),说明百秋李醇的确可作为广藿香饮片质量控制和优劣评价的指标之一。同时,研究发现广藿香即使不含叶只有梗,其百秋李醇含量也能达到中国药典标准规定的0.10%,而按照正常叶比例投料,规范生产的广藿香饮片百秋李醇含量应在0.30%以上。说明现行药典标准百秋李醇含量测定限度制定太低,应该按照规范生产的叶比例范围提高其限度[14]。在含量测定指标的寻找和确立方面,选定并确立与质量相关的指标非常关键。广藿香同时含有广藿香酮和百秋李醇等多种成分,藿香酮虽然也为广藿香中专属性成分,但研究发现广藿香酮仅存在于梗中,而叶中几乎没有,而百秋李醇则在梗和叶中均有,而在叶中含量更高(图5)。因此,百秋李醇作为广藿香药材及饮片质量控制和评价指标更为科学合理。
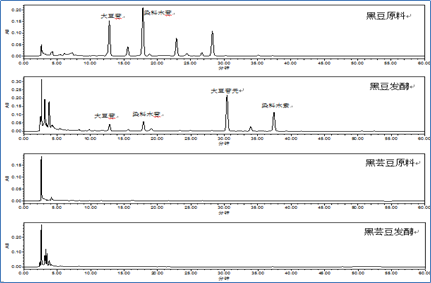
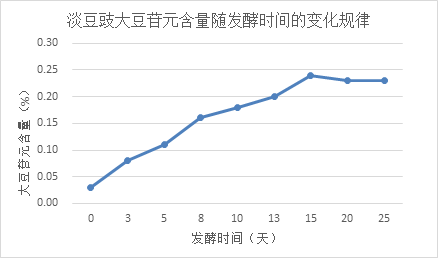
另外,质量指标的选择除了考虑与质量的相关性外,尽量选择专属性强的指标成分,对于中药饮片,质量指标应尽力体现炮制工艺对药材的改变及程度。以淡豆豉质量指标的发现和确立为例,2019年国家饮片抽检工作发现市场上有近40%的淡豆豉饮片不合格,主要原因为原料掺伪和发酵时间不够[15]。掺伪主要是采用价格更便宜的黑芸豆投料,而非《中国药典》规定的黑豆;按照生产工艺,淡豆豉需经两次发酵约20d左右才能完成,但部分样品存在发酵时间不够,偷工减料的情况。为控制淡豆豉饮片的真伪投料和发酵程度,经研究发现黑豆含有伪品黑芸豆所不含的大豆异黄酮类成分,且在发酵过程中,大豆异黄酮苷类成分可在生物酶的作用下转化为苷元,大豆苷元含量可伴随发酵时间呈现逐步升高至平稳的状态(图6)。因此,大豆苷元可以用于鉴别淡豆豉生产所用原料的真实性,其含量亦可以作为其发酵程度的关键指标。通过确立大豆苷元为质量指标并制定合理的限度来提升淡豆豉质量的方法已收入2020年版《中国药典》一部,不失为专属性强,简单又管用的标准。
A
B
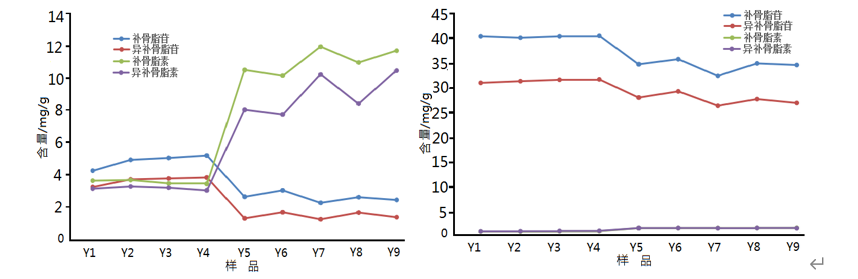
补骨脂的标准也存在指标选择合理性方面的问题,原标准只选取其所含的香豆素苷元类成分(补骨脂素和异补骨脂素)作为含量测定指标成分来控制补骨脂药材及饮片的质量,行业内发现补骨脂新货含量测定不合格率较高,而陈货的含量容易合格,因此有了“新货捂一捂即能合格”的潜规则,但陈货久置容易导致成分变化或容易霉变导致黄曲霉毒素超标,安全风险大。另外,民间流传补骨脂“越瘪越好”,因发现未成熟、不饱满、外形干瘪的补骨脂反而按药典标准测定含量更高。经过研究发现,补骨脂在放置过程中其所含的补骨脂苷类成分在酶的作用下慢慢转化为苷元类成分补骨脂素和异补骨脂素,因而随着放置年限增加,久置陈货含量测定更容易合格。补骨脂苷和异补骨脂苷的含量主要分布在种仁里,补骨脂素和异补骨脂素含量主要分布在皮里,且随着存储年限的增加,皮里的补骨脂苷和异补骨脂苷的含量明显下降,补骨脂素和异补骨脂素含量明显增加,种仁里的补骨脂苷、异补骨脂苷明显下降,但补骨脂素和异补骨脂素含量均变化不甚明显,因而也解释了“越瘪越好”的说法(图7)。为此在标准修订时将含量指标改为总补骨脂类成分,即样品经酸水解后测定苷元(补骨脂素、异补骨脂素)的总和,从而避免所含成分随放置时间变化的情况,这样不仅克服了行业内只能使用陈货的弊病,而且质量控制更加全面,也提高了药品的安全性[16-17]。该标准修订草案已经药典委员会采纳并公示。
A B
总之,中药材及饮片质量标准制定应坚持中药材质量特点,围绕质量属性确立质量指标,制定管用的标准。质量指标的选择和确立,应紧扣道地性和生产规范性这两大质量属性形成的关键条件和影响因素,在充分的因素分析和比对验证的基础上,尽可能选择质量相关性强、专属性强、代表性好、稳定性好、可行性强的指标和方法。体现中药材及饮片来源的正确性和真实性、生产过程的规范性,从而保证产品的安全性、有效性、稳定性和一致性。
3.2.3守住真伪和安全底线,基于风险评估,制定安全标准
中药和化学药品不同,因其功效作用的发挥相对缓慢,而且有不少属于药食同源的中药,消费者需要长期大量服用。因此,其真伪和安全性问题是质量风险最大,公众最为关心,也是市场质量监管的首要关注和底线要求。基于安全性的质量控制指标包括外源性有害残留(包括重金属及有害元素、农药残留、二氧化硫残留、真菌毒素、其他环境污染物等)和内源性有毒物质(中药材本身含有的一些有毒化学成分如乌头碱类、马钱子碱、罂粟碱类、马兜铃酸类、吡咯里西啶生物碱类等)。外源性有害残留属于环境污染物或种植加工中人为引入的有毒物质,需基于风险评估制定科学合理的限量标准。有些内源性有毒物质本身也是有效成分,因此在饮片炮制时对这些成分应特别关注,须制定适宜的含量限度范围,用法用量及包装贮藏方面亦应当严格规定。中药存在同名异物、同物异名的情况,形态相似的近缘种、近似种也较多,真伪问题一直是中药材及饮片质量控制和市场监管的重点,针对掺杂使假而建立的真伪鉴别方法是中药标准中最为常见的项目。近年来,分子生物学技术、色谱和质谱技术的发展和相应的特征图谱方法应用于中药标准,大大丰富了中药传统鉴别手段,也解决了长期难以解决的真伪鉴别难题。如液质联用特征肽段鉴别方法解决了阿胶掺伪牛皮和马皮等杂皮的技术难题[18-19],PCR鉴别方法可以有效区分川贝母和常见伪品[20]。真伪鉴别方法最为关键的就是指标和方法应专属性强,科学实用。例如近年来,一些地方因薄荷品种鉴定有误,将薄荷同属的近似种留兰香误认为薄荷大规模种植,并以此为原料生产薄荷饮片。从外观看二者性状极为相似,难以区分(图8)。原药典标准薄层鉴别法专属性不强,无法有效控制薄荷中留兰香的掺伪。化学成分比较研究发现,薄荷和留兰香所含化学成分差异大,薄荷含有大量的薄荷脑,而留兰香含有很少的薄荷脑,但含有大量的香芹酮类成分(图9)。围绕特征性成分建立的新的薄层鉴别方法及新增的薄荷脑含量测定项,专属性明显提高,可有效鉴别和控制薄荷药材和饮片中留兰香的掺伪,该修订标准已被收入2020年版《中国药典》一部[21-22]。


4.中药材及饮片质量标准研究应注意的几个问题和常见误区
中药材及饮片标准研究制修订以及标准在使用过程中经常会出现一些不同的观点和争议,有些的确属于科学问题,需要进一步深入研究;有些其实属于对标准及标准化工作理解不当,或对中药质量的认识和理解不够造成的。以下几个方面代表性的问题或误区值得思考,在标准研究制定时应引起重视。
4.1药材可药用基原并非都需收入标准
中药材的基原是其标准来源项下最为根本的内容。在中药材标准研究制定工作中,基原的确定通常要考虑多方面的因素,包括其临床使用历史、本草记载和考证、资源分布情况、市场流通和使用情况、人工抚育技术可行性及产业化情况以及生物多样性保护和资源可持续利用等相关考量。在中药材资源的有效利用方面,古今差别较大,古人多以野生资源并就地取材为主,同时也没有现代植物分类学的物种区分依据,组织化程度低,规范化管理少。随着社会发展、技术进步、生产方式转变、需求增加以及野生资源使用日益受限,现在常用大品种中药材多以人工抚育为主,集约化、机械化、规范化生产的要求随之加强,因此必须走标准化的道路。因此,基于“共同性” “统一性” “重复性” “一致性” “协调性”等原则的中药标准制定和标准化管理手段应运而生。按照中医临床就地取材用药传统,考虑到不同物种的地域分布特点,同一中药在不同地区所使用的基原肯定会有不同,很难将传统中药品名与现代意义上的基原物种一一对应和关联,给研究标准制定工作中基原的确立带来很多困难。因此,对于使用地域宽广、使用历史悠久、使用方式丰富的这样一个中医药大国,在制定国家标准时,基原的确定往往很难。一是难以确定正确的基原,二是在基原的扩充或取舍方面难以平衡协调。因此行业内经常会有对标准收载基原的合理性、准确性方面的争论和质疑声音,诸如“古人就地取材,同属多基原药材都可药用,国家标准只收载一两个基原不合理”等议论一直存在。
通常,中药材标准是基于质量控制目的,为适应标准化管理需求而制定的。无标准或未收入中药材标准者不能说就不是中药或不能药用,中药大辞典等方书典籍中收录了大量的无标准的中药,应该也是可以使用的,只是暂未纳入标准化管理而已。标准的制定不仅是提升中药材质量稳定、均一的技术手段,同时更是引导和鼓励规模化、规范化人工种植,加强药材资源保护的重要举措。过去曾经有过一些药材,标准规定了明确的基原,但因产业界未开展人工种植,其野生资源经长期采挖导致濒临枯竭,然后提出对标准来源项修订,更换为同属另一种资源相对丰富的基原,结果没过几年新基原的药材资源也濒临灭绝了,这些都是沉痛的教训。不能因为资源紧缺了就通过修订标准的手段扩充基原,对于大规模、工业化使用的药材资源,必须要加强和推进人工种植,不能依赖野生资源。从这个意义上讲,将石斛“同属近似种”都收入国家标准的做法不妥,不仅不符合标准化的理念,更不利于有限的石斛野生资源和生物多样性的保护。因此,促进对自然资源的保护和合理利用,维护人类社会当前和长远的利益,这也是我们国家中药材标准在基原遴选时应综合考量的关键问题,应该尽快研究制定中药材基原收入的指导原则。另外,随着科技进步和认识水平的提高,以及经济全球化的日益发展,我们在制定标准时也要有国际视野,对国外可利用的资源如苏合香、乳香、没药、紫草等,应该加强调查和研究,在制定我国国家标准时,可借鉴一些国际标准的内容和现代研究成果。
4.2活性成分不一定就是合理的质量指标
质量控制应该选择功效成分为指标,因此选择活性成分本无可厚非,但每味中药成分复杂多样,几乎每一种化学成分或多或少具有这方面或那方面的活性,甚至有很多活性我们只是暂时还不知道而已。因此选择质量控制评价指标时,应该优先考虑和质量属性最相关的成分作为指标,而不宜过分依赖于某些成分的个别活性,也不要发现了某个化学成分有新的某方面活性,就以此成分为指标增加一个含量测定项。更有甚者,不管成分有没有活性,也不管其与质量相不相关,将有没有可获得的对照品作为选择质量指标的决定性因素,这些都是不可取的。忽视指标和质量之间的相关性,过分追求活性成分,倚重或趋鹜于某一个成分的某一方面活性,对于中药的质量控制和评价来说都属于强调个性而忽略了整体的片面做法。
4.3标准研究不宜片面追求新技术新方法
只要能满足质量控制要求,中药标准应以简便、经济、实用为宜,不是技术方法越新、测定成分指标越多就认为标准水平高。标准不应成为新技术、新方法的堆砌。行业内曾经存在一些片面的认识,多认为“没有含量测定项,标准太低”、“多增加一个含量测定指标成分,以提高标准水平”“过去测一个成分,现在改用一测多评法大大提高了质量控制水平”。这些认识过分强调了技术和方法,忽视了质量标准用于控制和评价药品质量的初衷,盲目追求新技术、新方法、新仪器。简单便捷的理化小实验能解决的问题非要用高端大型仪器。因此不要为了一测多评而一测多评、为了多成分含量测定而含量测定,与质量无关或重复多余的指标宁可不纳入标准。另外,一些新的技术手段、少常用的方法、大型仪器的应用,要考虑方法和仪器的普及程度,以及基于成本效益评估其合理性和可行性。另外,不宜将现代科学技术的新发现、新创造、新成果急于体现在药材标准里,如因为发现了“新的活性成分”就作为创新成果来替换原标准的质控指标,这些做法不妥。中药材质量指标的确立不仅应考虑其科学性、合理性、可行性,还应保持相对的稳定性。中药材是饮片的原料,同时饮片又是中成药及许多健康相关产品的原料。原料质量控制指标的改变会影响到众多制剂产品质量控制和标准制定。因此,饮片和制剂质量指标应该和药材质量指标建立相关性和可追溯性。
4.4不宜片面强调个别标准质控指标的作用
标准中的质量指标是在规范生产前提下研究确立的质量属性相关性指标,不适合于非规范生产的产品的质量评价。同时,产品的质量是多维度、多属性、多指标的综合体现,个别质量指标高不一定说明其质量就好。然而,对于行业内质量意识薄弱的从业者,标准中的关键指标变成了制定生产规范的依据,“符合标准指控指标”成为生产企业的奋斗目标,通过生物技术等现代高新技术手段提高标准中某些指标成分的含量成为部分科研工作者开发“高质量”中药的方向。因此,不能围绕药典标准的个别指标值的提高而盲目修改既定的生产规范,或者为了让个别质控指标含量升高而改变传统种植产地、改变种和采收加工植方式。更不宜围绕《中国药典》确定的含量测定指标大做文章,如出现过采用基因改变等生物技术或干预措施让药材的个别指标成分含量升高的做法,这些都是脱离中医药传统理论的做法。
4.5标准研究应该使用来源清楚的代表性样品,而不是随机的市场样品
好多针对中药材标准可行性差的问题,如特征描述不恰当、鉴别专属性不够、限度制定不合理等问题,都跟标准研究时选用样品的代表性不够有关。样品代表性是标准制定科学性、合理性及可行性的关键。与中药制剂及其他药品标准的研究相比,中药材及饮片因其天然来源,质量受产地和自然环境因素影响大,样品均匀性和批次一致性较差,因此标准研究中要非常注重样品的代表性,其产地、种植/养殖方式、药用部位、采收季节、采收加工方法等均应明确,多基原的药材还应具体明确是哪种基原。通常标准研究技术要求不少于15批次的研究样品,但要考虑的多方面的代表性,应该尽可能选择多于15批次的代表性样品。必要时还需人为或专门收集一些欠规范生产、掺杂使假、特定生产工艺和条件、或不同影响因素及质量相关的样品,用于质量指标的确定、方法建立、限度制定和相关比较研究。因此样品的代表性往往是标准制定成败的关键,是标准研究工作必须引起高度重视和首要解决的问题。
5.构建全面的中药材质量控制和评价标准体系,助推中药整体质量提升
5.1加强源头控制和规范生产
质量源于生产,中药质量的源头即为中药材的生产,源头控制是中药质量提升的根本和关键举措。积极鼓励推动中药材规范化种植是一个复杂的系统工程,其具有农业生产的基本特性,同时又具有药品生产的基本属性。中药材的产区具有道地性,而在长期的种植过程中,药材的道地性逐渐被淡忘,除了道地产区,非道地产区的引种已广泛存在。同时,我国中药材生产种植仍存在非法使用违禁农药、超量使用农药及植物生长调节剂类产品的现象,种植集约化程度低,难以实行统一的标准化和规范化操作,导致药农田间管理成本高、产量低。药材中的农药残留超标严重、内在成分含量低,中药材质量无法得到有效保障。因此,首先要考虑药材产区的道地性,鼓励在道地产区或适宜产区进行引种,要全面建立药材的种植/养殖生产规范,并开展规范化的生产加工。鼓励中药材生态化、规范化种植,建立绿色可持续发展理念,从源头上提升中药材的质量和安全。近期,国家药监局、农业农村部、国家林草局、国家中医药局联合发布《中药材生产质量管理规范》(GAP),用于中药材生产企业规范生产中药材的全过程管理,是中药材规范化生产和管理的基本要求[23]。GAP的发布是贯彻落实《中共中央国务院关于促进中医药传承创新发展的意见》,推进中药材规范化生产,加强中药材质量控制,促进中药高质量发展的重要举措。
5.2构建全链条各环节生产技术规范和标准体系
GAP是共性的指导原则性质的规定,而对于每一个具体中药材品种,目前缺乏适合各品种特点的生产技术规范、操作规程和相应的质量控制标准。因此,应考虑建立全链条、全要素规范体系的重要性和必要性,系统构建和完善中药质量标准技术体系。如建立具体品种中药材种子种苗繁育体系技术规范、种植(养殖)技术规范、药材产地加工技术规范、中药材及饮片贮存、养护与包装、运输等技术规范,用技术规范指导生产实践,用技术规范引领产业的良好发展,最终达到中药材及中药饮片质量可追溯、可控制,实现全产业链的稳定、有序发展。
5.3积极探索质量优劣评价方法和质量等级标准制定
长期以来,中药质量评价只有底限,即中国药典中规定的基本标准,没有评判质量优劣的等级标准,因为中药材的质量受自然环境和人为干预影响很大,其质量等级是客观存在的。质量等级标准是评价质量优劣,维护市场公平和公正的有力工具。传统上,中药材在商品上的等级划分,是根据不同产地、重量、大小等因素确定的,然而,随着中药产业的迅速发展,中药材及饮片传统商品规格等级划分已经不能很好的与其质量关联,商品规格等级无法满足种植中药材的质量评价要求。产品的质量仅以中国药典进行低限控制,致使优质药材和劣质药材均符合药典规定,体现不出优质药材的优势。究其原因,主要是由于整个行业缺少以质量与安全为核心的等级评价标准,缺乏评价中药材及饮片生产规范程度和水平高低的认证标准,导致优质优价难以体现,劣币驱逐良币,市场公平和公正严重受损,严重影响到中药产业的健康发展。因此,构建中药材质量等级标准体系,推行中药材质量评价和质量等级优劣认证,对规范市场秩序、推优驱劣,引导和督促产业发展,驱动行业内部结构调整和升级,树立优质品牌,做强做大中药产业,保障中药产业健康有序发展具有重要的现实意义,也是道地药材规范化种植行动及基地产品市场生命力的有力保障。总之,中药的质量是其防病治病、安全有效的保证,质量和安全问题不解决,则中药产业发展及中医药事业难以为继;质量评价标准不建立,则公平公正、规范有序的市场体系无法保障,中药优质产品难以培育。以药材道地性和规范生产基地建设为引擎,加强创新研究和保障体系建设,构建中药材质量等级标准体系,势必会对解决中药行业质量问题、提升产业发展水平,促进中医药事业发展产生深远的影响,对传承好、利用好、发展好祖国中医药事业具有基础性和根本性的意义。
总之,中药材及饮片标准研究是一个系统复杂的工程,有赖于基础研究和临床认知的不断深入。在开展标准研究和制修订时,围绕中药材质量属性形成的关键要素,寻找、发现、并确立与质量密切相关的质量指标最为关键。为此,必须坚持中医药特点,基于中医临床质量认知,制定有效的标准;坚持中药材质量特点,围绕质量属性确立关键质量指标,制定管用的标准;特别是要守住真伪和安全底线,基于风险评估,制定安全的标准。中药的质量源于生产过程的规范性操作,而标准的提高完善又可以引导和促进规范生产。因而,加强中药材及饮片标准研究,不断提升和完善质量控制和评价标准,对推动中药产品质量提升和中药产业高质量发展具有重要的意义。



标签:
【免责声明】
1.“高鹏说药材”致力于提供中药行业各类资讯信息,但不保证信息的合理性、准确性和完整性,且不对因信息的不合理、不准确或遗漏导致的任何损失或损害承担责任。
2.“高鹏说药材”部分文章信息来源于网络转载是出于传递更多信息之目的,并不意味着赞同其观点或证实其内容的真实性。如对内容有疑议,请及时与我平台联系。
3.“高鹏说药材”所有信息仅供参考,不做任何商业交易及或医疗服务的根据,如自行使用“高鹏说药材”内容发生偏差,我平台不承担任何责任,包括但不限于法律责任,赔偿责任。
4.“高鹏说药材”各类带“原创”标识的资讯,享有著作权及相关知识产权,未经本网站协议授权,任何媒体、网站、个人不得转载、链接或其他方式进行发布;经本网协议授权的转载或引用,必须注明“来源:高鹏说药材(www.gpsyc.com)”。违者本网站将依法追究法律责任。
5.本声明未涉及的问题参见国家有关法律法规,当本声明与国家法律法规冲突时,以国家法律法规为准。
最新文章

百花农品:真药材,平价卖,守护千年药香
在中药材电商市场蓬勃发展的当下,乱象丛生:染色虫草、硫磺枸杞...(1080 )人阅读时间:2025-02-27
破茧重生:民间中医的千年传承亟需政策松绑!
中医,作为中华文明的瑰宝,数千年来以“简、便、验、廉”的特点...(926 )人阅读时间:2025-02-25
理性看待民间中医的作用:传承与困境中的“高手在民间”
中医作为中华文明的瑰宝,其生命力不仅存在于现代医疗体系内,更...(894 )人阅读时间:2025-02-24
让真药材回归百姓家——守护中药生态,百花农品与您同行!
中药,是中国人代代相传的健康密码,承载着“治未病”的智慧与自...(1025 )人阅读时间:2025-02-21


 概论中药材种植产业发展管理赵军 王振华 董秋梅 李林 赵智博...
概论中药材种植产业发展管理赵军 王振华 董秋梅 李林 赵智博...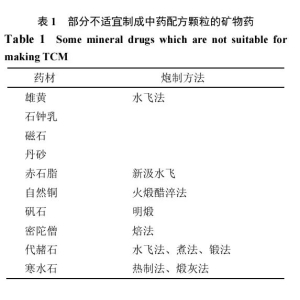 不适宜制备中药配方颗粒的中药材品种探讨王 晨 1,时 政 2...
不适宜制备中药配方颗粒的中药材品种探讨王 晨 1,时 政 2... 中药材种类繁多,药用部位不同,其最佳采收的时间也不相同。所谓...
中药材种类繁多,药用部位不同,其最佳采收的时间也不相同。所谓... 来源:《中国农学通报》2022,38(31)中药材农药残留研...
来源:《中国农学通报》2022,38(31)中药材农药残留研...


